| 全方位带您了解医疗器械UDI!(第九篇) | |
|
|
医疗器械事关人民生命健康。UDI作为医疗器械的身份证,第三类医疗器械已经要求全部覆盖,唯一标识将逐渐覆盖所有器械。为了更好的帮助大家了解UDI,小编针对大家都比较关心的重点问题进行了整理与解答,从基础知识、相关法规标准、实施过程及步骤、数据库使用、发码机构、后续应用等方面帮助大家更好的了解UDI体系脉络。今天和大家一起分享UDI科普问答第九篇,希望对小伙伴们有所帮助!(第一篇链接:第二篇链接:第三篇链接:第四篇链接:第五篇链接:第六篇链接:第七篇链接:第八篇链接:) 五、UDI 发码机构相关问答: 58.发码机构需要具备什么样的资质,其职责和义务有哪些? 器械唯一标识的发码机构应当为中国境内的法人机构,具备完善的管理制度和运行体系,确保按照其标准创建的医疗器械唯一标识的唯一性,并符合我国数据安全有关要求。发码机构应当向注册人/备案人提供执行其标准的流程并指导实施,为便于注册人/备案人等掌握发码机构的编码标准,供相关方选择或应用,发码机构应当将其编码标准上传至医疗器械唯一标识数据库并动态维护。每年 1月31日前,发码机构应当向国家药品监督管理局提交按照其标准创建的唯一标识上一年度的报告。(《医疗器械唯一标识系统规则》解读) 59.目前符合要求的发码机构有哪几家? 分别是“中国物品编码中心”、“中关村工信二维码技术研究院”和“阿里健康科技(中国)有限公司”。 60.三家发码机构对应的码制是什么? “中国物品编码中心”发行的代码为GS1码;“中关村工信二维码技术研究院”发行的代码为 MA 码;“阿里健康科技(中国)有限公司”发行的代码为 AHM码。 61.UDI-GS1码是主要由哪些信息组成的? 示例说明如下(可按规定做相应调整): DI:厂商识别代码由 7~10 位数字组成,中国物品编码中心负责分配和管理。厂商识别代码的前3位代码为前缀码,国际物品编码协会已分配给中国物品编码中心的前缀码为 690~699;商品项目代码由厂商识别代码所有人(即商品条码系统成员)依据有关国家标准自行分配;校验码由标准算法得出。 PI:包含医疗器械序列号、生产批号、生产日期、失效日期等。(基于商品条码(GS1)标准的医疗器械唯一标识(UDI)实施指南-中国物品编码中心) http://www.gs1cn.org/ 62.MA码是由哪些信息组成的? DI:由国家前缀码 3 位;行业标识符 2 位;注册人代码 6 位;包装指示符 1 位;产品代码 6 位;校验码 1 位组成。 PI:包含医疗器械序列号、生产批号、生产日期、失效日期等。(UDI 发码服务平台) 63.AHM码是由哪些信息组成的? 第一单元部分为产品资源码:追溯码前 7 位,包含企业信息、药品名称、剂型、批准文号、包装规格等信息,方便产品识别;第二单元部分为单件序列:追溯码 8到16位,是单件商品序列号;最后单元部分为校验位:追溯码17到20位,校验位由特殊加密算法生成。(“码上放心”追溯平台药品追溯码编码规范) 64.医疗器械唯一标识系统采用GS1码制时DI对应应用标识符是什么? DI主要为贸易项目应用标识符AI(01)的相应内容,应用标识符“01”对应的数据编码的含义为全球贸易项目代码(Global Trade Item Number,简称GTIN),贸易项目的GTIN包括GTIN-8,GTIN-12,GTIN-13或GTIN-14标识代码,数据编码格式见表。 UDI常规采用GTIN-14码制。(编码规则详见GB/T 16986-2018 商品条码_应用标识符) (行政审批处) |
|
| 【关闭本页】 【打印本页】 |
扫一扫在手机打开当前页
本站由江苏省药品监督管理局主办 版权所有未经许可禁止转载或者建立镜像
邮编:210008 电话:025-83273610 地址:南京市鼓楼街5号 政府网站标识码3200000004
备案号:苏ICP备09039606号 苏公网安备:32010602010488 您是第位访问者

医疗器械事关人民生命健康。UDI作为医疗器械的身份证,第三类医疗器械已经要求全部覆盖,唯一标识将逐渐覆盖所有器械。为了更好的帮助大家了解UDI,小编针对大家都比较关心的重点问题进行了整理与解答,从基础知识、相关法规标准、实施过程及步骤、数据库使用、发码机构、后续应用等方面帮助大家更好的了解UDI体系脉络。今天和大家一起分享UDI科普问答第九篇,希望对小伙伴们有所帮助!(第一篇链接:第二篇链接:第三篇链接:第四篇链接:第五篇链接:第六篇链接:第七篇链接:第八篇链接:)
五、UDI 发码机构相关问答:
58.发码机构需要具备什么样的资质,其职责和义务有哪些?
器械唯一标识的发码机构应当为中国境内的法人机构,具备完善的管理制度和运行体系,确保按照其标准创建的医疗器械唯一标识的唯一性,并符合我国数据安全有关要求。发码机构应当向注册人/备案人提供执行其标准的流程并指导实施,为便于注册人/备案人等掌握发码机构的编码标准,供相关方选择或应用,发码机构应当将其编码标准上传至医疗器械唯一标识数据库并动态维护。每年 1月31日前,发码机构应当向国家药品监督管理局提交按照其标准创建的唯一标识上一年度的报告。(《医疗器械唯一标识系统规则》解读)
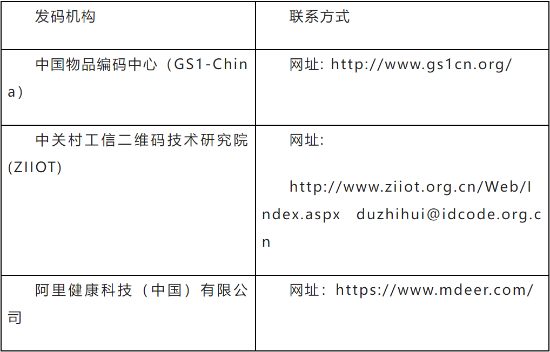
59.目前符合要求的发码机构有哪几家?
分别是“中国物品编码中心”、“中关村工信二维码技术研究院”和“阿里健康科技(中国)有限公司”。
60.三家发码机构对应的码制是什么?
“中国物品编码中心”发行的代码为GS1码;“中关村工信二维码技术研究院”发行的代码为 MA 码;“阿里健康科技(中国)有限公司”发行的代码为 AHM码。
61.UDI-GS1码是主要由哪些信息组成的?
示例说明如下(可按规定做相应调整):
DI:厂商识别代码由 7~10 位数字组成,中国物品编码中心负责分配和管理。厂商识别代码的前3位代码为前缀码,国际物品编码协会已分配给中国物品编码中心的前缀码为 690~699;商品项目代码由厂商识别代码所有人(即商品条码系统成员)依据有关国家标准自行分配;校验码由标准算法得出。 PI:包含医疗器械序列号、生产批号、生产日期、失效日期等。(基于商品条码(GS1)标准的医疗器械唯一标识(UDI)实施指南-中国物品编码中心) http://www.gs1cn.org/
62.MA码是由哪些信息组成的?
DI:由国家前缀码 3 位;行业标识符 2 位;注册人代码 6 位;包装指示符 1 位;产品代码 6 位;校验码 1 位组成。 PI:包含医疗器械序列号、生产批号、生产日期、失效日期等。(UDI 发码服务平台)
63.AHM码是由哪些信息组成的?
第一单元部分为产品资源码:追溯码前 7 位,包含企业信息、药品名称、剂型、批准文号、包装规格等信息,方便产品识别;第二单元部分为单件序列:追溯码 8到16位,是单件商品序列号;最后单元部分为校验位:追溯码17到20位,校验位由特殊加密算法生成。(“码上放心”追溯平台药品追溯码编码规范)
64.医疗器械唯一标识系统采用GS1码制时DI对应应用标识符是什么?
DI主要为贸易项目应用标识符AI(01)的相应内容,应用标识符“01”对应的数据编码的含义为全球贸易项目代码(Global Trade Item Number,简称GTIN),贸易项目的GTIN包括GTIN-8,GTIN-12,GTIN-13或GTIN-14标识代码,数据编码格式见表。
UDI常规采用GTIN-14码制。(编码规则详见GB/T 16986-2018 商品条码_应用标识符)
(行政审批处)
本站由江苏省药品监督管理局主办
版权所有未经许可禁止转载或者建立镜像
邮编:210008
电话:025-83273610
地址:南京市鼓楼街5号
政府网站标识码3200000004
备案号:苏ICP备09039606号
苏公网安备:32010602010488